2019-03-31 11:33:26

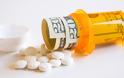
Σε ανάκληση φαρμακευτικών σκευασμάτων που χρησιμοποιούνται για τον έλεγχο της υπέρτασης προχωρά ο Εθνικός Οργανισμός Φαρμάκων (ΕΟΦ).
Πιο συγκεκριμένα, ο ΕΟΦ ανακαλεί την παρτίδα 150218 του φαρμακευτικού προϊόντος IRBESARTAN HYDROCHLOROTHIAZIDE/ACTAVIS (150+12.5) mg και την παρτίδα 263918 του φαρμακευτικού προϊόντος IRBESARTAN HYDROCHLOROTHIAZIDE/ACTAVIS (300+25) mg. Όπως αναφέρει ο ΕΟΦ, η παρούσα απόφαση αποτελεί προληπτικό μέτρο για την προάσπιση της Δημόσιας Υγείας κατόπιν ανίχνευσης, σε μια από τις παρτίδες δραστικής ουσίας ιρβεσαρτάνη που χρησιμοποιήθηκαν στις ανωτέρω παρτίδες τελικού προϊόντος, της ουσίας NDEA (πιθανός καρκινογόνος παράγοντας) σε επίπεδα άνω των επιτρεπτών ορίων.
Ο ΕΟΦ επισημαίνει ότι η εταιρεία SPECIFAR ΑΒΕΕ οφείλει να υλοποιήσει την ανάκληση σε εύλογο χρονικό διάστημα.
Παράλληλα, προχωρά και στην ανάκληση συγκεκριμένων παρτίδων (βλέπε τον παρακάτω πίνακα) των φαρμακευτικών προϊόντων PRESSDOWN 100 mg, PRESS-DOWN PLUS(100+25) mg και PRESS-DOWN PLUS (50+12,5) mg, διότι το πιστοποιητικό CEP της δραστικής ουσίας losartan που χρησιμοποιήθηκε για την παραγωγή των εν λόγω παρτίδων τελικού προϊόντος έχει ανακληθεί και δεν προσκομίστηκαν αποτελέσματα εργαστηριακών ελέγχων για τις NDEA/NDMA από τον Κάτοχο Άδειας Κυκλοφορίας.
Και σε αυτήν την περίπτωση, ο ΕΟΦ αναφέρει ότι η παρούσα απόφαση εκδίδεται προληπτικά στο πλαίσιο προάσπισης της δημόσιας υγείας, σημειώνοντας ότι η εταιρεία PHARMAZACΕΠΕ οφείλει να επικοινωνήσει άμεσα με τους αποδέκτες των συγκεκριμένων παρτίδων και να τις αποσύρει από την αγορά μέσα σε εύλογο χρονικό διάστημα.
_
bloko
Πιο συγκεκριμένα, ο ΕΟΦ ανακαλεί την παρτίδα 150218 του φαρμακευτικού προϊόντος IRBESARTAN HYDROCHLOROTHIAZIDE/ACTAVIS (150+12.5) mg και την παρτίδα 263918 του φαρμακευτικού προϊόντος IRBESARTAN HYDROCHLOROTHIAZIDE/ACTAVIS (300+25) mg. Όπως αναφέρει ο ΕΟΦ, η παρούσα απόφαση αποτελεί προληπτικό μέτρο για την προάσπιση της Δημόσιας Υγείας κατόπιν ανίχνευσης, σε μια από τις παρτίδες δραστικής ουσίας ιρβεσαρτάνη που χρησιμοποιήθηκαν στις ανωτέρω παρτίδες τελικού προϊόντος, της ουσίας NDEA (πιθανός καρκινογόνος παράγοντας) σε επίπεδα άνω των επιτρεπτών ορίων.
Ο ΕΟΦ επισημαίνει ότι η εταιρεία SPECIFAR ΑΒΕΕ οφείλει να υλοποιήσει την ανάκληση σε εύλογο χρονικό διάστημα.
Παράλληλα, προχωρά και στην ανάκληση συγκεκριμένων παρτίδων (βλέπε τον παρακάτω πίνακα) των φαρμακευτικών προϊόντων PRESSDOWN 100 mg, PRESS-DOWN PLUS(100+25) mg και PRESS-DOWN PLUS (50+12,5) mg, διότι το πιστοποιητικό CEP της δραστικής ουσίας losartan που χρησιμοποιήθηκε για την παραγωγή των εν λόγω παρτίδων τελικού προϊόντος έχει ανακληθεί και δεν προσκομίστηκαν αποτελέσματα εργαστηριακών ελέγχων για τις NDEA/NDMA από τον Κάτοχο Άδειας Κυκλοφορίας.
Και σε αυτήν την περίπτωση, ο ΕΟΦ αναφέρει ότι η παρούσα απόφαση εκδίδεται προληπτικά στο πλαίσιο προάσπισης της δημόσιας υγείας, σημειώνοντας ότι η εταιρεία PHARMAZACΕΠΕ οφείλει να επικοινωνήσει άμεσα με τους αποδέκτες των συγκεκριμένων παρτίδων και να τις αποσύρει από την αγορά μέσα σε εύλογο χρονικό διάστημα.
_
bloko
ΦΩΤΟΓΡΑΦΙΕΣ
ΜΟΙΡΑΣΤΕΙΤΕ
ΔΕΙΤΕ ΑΚΟΜΑ
ΠΡΟΗΓΟΥΜΕΝΟ ΑΡΘΡΟ
Πρόεδρος ΣΦΕΕ: Οι φαρμακευτικές έχουν γίνει χρηματοδότες της υγείας
ΣΧΟΛΙΑΣΤΕ