2021-10-09 10:25:55

Οι Benjamin List και David MacMillan βραβεύθηκαν με το Νόμπελ Χημείας 2021 για την ανάπτυξη ενός νέου και ευφυούς εργαλείου για τη δημιουργία μορίων: την οργανοκατάλυση. Πρόκειται για καταλύτες που είναι εύχρηστοι, φθηνοί και αποδοτικοί στην ασύμμετρη κατάλυση με εφαρμογές στην βιομηχανία και στην παρασκευή φαρμακευτικών προϊόντων. Επιπλέον βοήθησαν την χημεία να γίνει πιο φιλική στο περιβάλλον.
Η βιομηχανική παραγωγή και πολλά πεδία έρευνας εξαρτώνται από την ικανότητα των χημικών να κατασκευάζουν νέα και εξειδικευμένα μόρια. Αυτά μπορεί να είναι οτιδήποτε, από ουσίες που συλλαμβάνουν φως στα φωτοβολταϊκά ή αποθηκεύουν ενέργεια σε μπαταρίες, μέχρι μόρια που χρησιμεύουν στην κατασκευή ελαφρών αθλητικών παπουτσιών ή αποτελούν συστατικά φαρμάκων που θεραπεύουν. Ωστόσο, αν περιμέναμε από την φύση να δημιουργήσει τα εξειδικευμένα μόρια που μας είναι χρήσιμα θα είχαμε μείνει στην ‘λίθινη’ εποχή.
Είναι γεγονός ότι η φυσική εξέλιξη δημιούργησε εκπληκτικά εξειδικευμένα εργαλεία, τα ένζυμα. Τα ένζυμα στους ζωντανούς οργανισμούς χρησιμεύουν για την κατασκευή των μοριακών συμπλεγμάτων που δίνουν στη ζωή τα σχήματα, τα χρώματα και τις λειτουργίες της. Αρχικά, όταν οι χημικοί απομόνωσαν αυτά τα χημικά αριστουργήματα, απλώς τα κοίταξαν με θαυμασμό. Σήμερα όμως, μπορούμε να πούμε ότι οι χημικοί ξεπέρασαν την φύση όσον αφορά τα εξειδικευμένα εργαλεία για την κατασκευή μορίων.
Νέα εργαλεία για καλύτερη χημεία
Η ανακάλυψη που τιμήθηκε με το βραβείο Νόμπελ Χημείας 2021 οδήγησε την τεχνητή κατασκευή μορίων σε ένα εντελώς νέο επίπεδο. Δεν έκανε μόνο τη χημεία πιο οικολογική, αλλά βελτίωσε σημαντικά την παραγωγή ασύμμετρων μορίων.
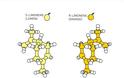
Πολλά μόρια εμφανίζονται σε δύο παραλλαγές, με την μόνη διαφορά ότι είναι κατοπτρικά συμμετρικά – το ένα είναι το είδωλο του άλλου στον καθρέφτη. Υπάρχουν κι άλλα αντικείμενα που παρουσιάζουν αυτή τη σχέση ειδώλου προς αντικείμενο όπως π.χ. τα χέρια μας. Δεν μπορούμε να βάλουμε ακριβώς το δεξιό μας χέρι πάνω στο αριστερό – μόνο στον καθρέφτη ταιριάζουν απόλυτα. Τα σώματα αυτά ονομάζονται χειρόμορφα ή χειρικά. Στην χημεία χειρόμορφα μόρια ονομάζονται τα μόρια τα οποία δεν ταυτίζονται με το κατοπτρικό τους είδωλο. Αυτό σημαίνει ότι μια ένωση της οποίας το μόριο είναι χειρόμορφο εμφανίζεται σε δύο μορφές, τα εναντιομερή. Τα μόρια αυτά ενώ έχουν τον ίδιο μοριακό τύπο, εμφανίζουν διαφορές στις φυσικές και χημικές ιδιότητές τους. Αυτό είναι ένα είδος ισομέρειας – για την ακρίβεια στερεοϊσομέρειας – που ονομάζεται εναντιομέρεια. Για παράδειγμα τα εναντιομερή του λεμονένιου: η μια εκδοχή του μορίου λεμονένιου έχει άρωμα λεμονιού, ενώ το κατοπτρικό του είδωλο μυρίζει πορτοκάλι!
Κατά την χημική αντίδραση για την παραγωγή ενός μορίου προκύπτει συχνά μια κατάσταση όπου μπορούν να σχηματιστούν δύο μόρια με τον ίδιο μοριακό τύπο, τα οποία – όπως και τα χέρια μας – είναι κατοπτρικά συμμετρικά. Οι χημικοί συνήθως θέλουν μόνο το ένα από τα δύο, κυρίως όταν παράγουν φαρμακευτικά προϊόντα. Όμως, ήταν δύσκολο να βρεθούν αποτελεσματικές μέθοδοι για να γίνει αυτό. Η ιδέα που αναπτύχθηκε από τους Benjamin List και David MacMillan – η ασύμμετρη οργανοκατάλυση – είναι τόσο απλή όσο και ευφυής. Είναι γεγονός ότι πολλοί άνθρωποι αναρωτήθηκαν γιατί δεν το σκεφτήκαμε νωρίτερα. Αυτό δεν είναι εύκολο να απαντηθεί, αλλά πριν το επιχειρήσουμε θάπρεπε να κάνουμε μια γρήγορη αναδρομή στην ιστορία. Θα ορίσουμε τις έννοιες κατάλυση και καταλύτης που είναι βασικές για την κατανόηση του Νόμπελ Χημείας 2021.
Οι καταλύτες επιταχύνουν τις χημικές αντιδράσεις
Τον δέκατο ένατο αιώνα, όταν οι χημικοί άρχισαν να διερευνούν τους τρόπους με τους οποίους οι διαφορετικές χημικές ουσίες αντιδρούν μεταξύ τους, έκαναν μερικές παράξενες ανακαλύψεις. Για παράδειγμα, όταν έβαζαν άργυρο σε ένα ποτήρι με υπεροξείδιο του υδρογόνου (H2O2), το υπεροξείδιο του υδρογόνου άρχιζε ξαφνικά να διασπάται σε νερό (H2O) και οξυγόνο (O2). Αλλά ο άργυρος – που ξεκίνησε την χημική αντίδραση – δεν φαινόταν να επηρεαζόταν καθόλου από από αυτή. Η τελική του ποσότητα παράμενε εντελώς ίδια με την αρχική. Το 1835, ο διάσημος Σουηδός χημικός Jacob Berzelius διαπίστωσε κι άλλα τέτοια παραδειγματα.
Σύμφωνα με τα σχολικά βιβλία: Καταλύτης ονομάζεται μια ουσία, η οποία με την παρουσία του σε μικρά ποσά, αυξάνει την ταχύτητα μιας αντίδρασης, ενώ στο τέλος της αντίδρασης παραμένει ουσιαστικά αμετάβλητος τόσο στη μάζα όσο και στη χημική του σύσταση.
Έτσι, στην ετήσια έκθεση της Βασιλικής Σουηδικής Ακαδημίας Επιστημών, όπου περιέγραφε τις τελευταίες προόδους στη φυσική και την χημεία, αναφέρεται σε μια νέα «δύναμη» που μπορεί να «δημιουργήσει χημική δραστηριότητα». Παρέθεσε αρκετά παραδείγματα στα οποία απλώς η παρουσία μιας ουσίας ξεκινούσε μια χημική αντίδραση, αναφέροντας πώς αυτό το φαινόμενο πρέπει να είναι πολύ πιο συνηθισμένο από ό,τι πιστεύαμε. Θεωρούσε ότι η ουσία είχε καταλυτική δύναμη και ονόμασε το ίδιο το φαινόμενο κατάλυση.
Οι καταλύτες παράγουν πλαστικά, αρώματα και νόστιμα τρόφιμα
Από την εποχή του Berzelius μέχρι σήμερα κύλισε πολύ νερό μέσα από τους δοκιμαστικούς σωλήνες των χημικών. Ανακαλύφθηκε πληθώρα καταλυτών που μπορούν να διασπούν ή να ενώνουν μόρια μεταξύ τους, δημιουργώντας χιλιάδες διαφορετικές ουσίες που χρησιμοποιούνται στην καθημερινή μας ζωή, όπως φαρμακευτικά προϊόντα, πλαστικά, αρώματα και καρυκεύματα τροφίμων. Είναι γεγονός ότι το 35% του συνολικού παγκόσμιου ΑΕΠ περιλαμβάνει κατά κάποιο τρόπο την χημική κατάλυση.
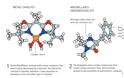
Όλοι οι καταλύτες που είχαν ανακαλυφθεί πριν από το 2000 ανήκαν σε δύο ομάδες: ήταν είτε μέταλλα είτε ένζυμα. Τα μέταλλα είναι συχνά εξαιρετικοί καταλύτες επειδή έχουν την ικανότητα να δέχονται προσωρινά ηλεκτρόνια ή να τα παρέχουν σε άλλα μόρια κατά τη διάρκεια μιας χημικής διαδικασίας. Αυτό βοηθά στην χαλάρωση των δεσμών μεταξύ των ατόμων σε ένα μόριο, έτσι ώστε οι δεσμοί που κατά τα άλλα είναι ισχυροί να σπάσουν και να σχηματιστούν νέοι.
Ωστόσο, ένα πρόβλημα με ορισμένους μεταλλικούς καταλύτες είναι ότι είναι πολύ ευαίσθητοι στο οξυγόνο και στο νερό, οπότε, για να λειτουργήσουν, χρειάζονται ένα περιβάλλον χωρίς οξυγόνο και υγρασία. Αυτό είναι δύσκολο να επιτευχθεί σε βιομηχανίες μεγάλης κλίμακας. Επίσης, πολλοί μεταλλικοί καταλύτες είναι βαρέα μέταλλα, τα οποία μπορεί να είναι επιβλαβή για το περιβάλλον.
Οι καταλύτες της ζωής λειτουργούν με εκπληκτική ακρίβεια
Η δεύτερη μορφή καταλύτη είναι τα ένζυμα που αποτελούνται από πρωτεΐνες. Όλα τα έμβια όντα διαθέτουν χιλιάδες διαφορετικά ένζυμα που ενεργοποιούν και καθοδηγούν τις χημικές αντιδράσεις που είναι απαραίτητες για την ζωή. Η παρουσία των ενζύμων αυξάνει την ταχύτητα αυτών των αντιδράσεων έως και 100 εκατομμύρια φορές. Αυτό πρακτικά σημαίνει ότι αντιδράσεις που πραγματοποιούνται, με την παρουσία ενζύμων, μέσα σ’ ένα λεπτό, θα χρειάζονταν 32 μήνες για να πραγματοποιηθούν χωρίς αυτά.
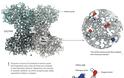
Πολλά ένζυμα είναι εξειδικευμένα στην ασύμμετρη κατάλυση και επιτρέπουν πάντα εξ’ ορισμού τον σχηματισμό ενός από τα δυο εναντιομερή. Λειτουργούν επίσης και διαδοχικά – αν ένα ένζυμο τελειώσει με μια αντίδραση, ένα άλλο παίρνει την σκυτάλη. Με αυτόν τον τρόπο, δημιουργούν περίπλοκα μόρια με εκπληκτική ακρίβεια, όπως η χοληστερόλη, η χλωροφύλλη ή η τοξίνη που ονομάζεται στρυχνίνη, η οποία είναι ένα από τα πιο πολύπλοκα μόρια που γνωρίζουμε (θα επανέλθουμε σε αυτό).
Επειδή τα ένζυμα είναι τόσο αποτελεσματικοί καταλύτες, οι ερευνητές στη δεκαετία του 1990 προσπάθησαν να αναπτύξουν νέες παραλλαγές ενζύμων για να ελέγχουν τις χημικές αντιδράσεις που χρειάζεται η ανθρωπότητα. Η ερευνητική ομάδα που εργάστηκε σ’ αυτό καθοδηγήθηκε από τον Carlos F. Barbas III στο Ινστιτούτο Ερευνών Scripps στη νότια Καλιφόρνια. Ο Benjamin List κατείχε μια μεταδιδακτορική θέση στην ερευνητική ομάδα του Barbas όταν γεννήθηκε η λαμπρή ιδέα που οδήγησε σε μία από τις ανακαλύψεις που βρίσκεται πίσω από το φετινό Νόμπελ Χημείας.
Το επαναστατικό αποτέλεσμα της σκέψης του Benjamin List
Ο Benjamin List εργάστηκε με καταλυτικά αντισώματα. Κανονικά, τα αντισώματα προσκολλώνται σε ξένους ιούς ή βακτήρια στο σώμα μας, αλλά οι ερευνητές στο Scripps τα επανασχεδίασαν ώστε να μπορέσουν να προκαλέσουν χημικές αντιδράσεις.
Κατά την διάρκεια της εργασίας του με καταλυτικά αντισώματα, ο Benjamin List άρχισε να προβληματίζεται για το πώς πραγματικά λειτουργούν τα ένζυμα. Είναι συνήθως τεράστια μόρια που κατασκευάζονται από εκατοντάδες αμινοξέα. Εκτός από αυτά τα αμινοξέα, ένα σημαντικό ποσοστό ενζύμων έχει επίσης μέταλλα που βοηθούν στην επιτάχυνση των χημικών διεργασιών. Αλλά – κι εδώ είναι το ζουμί – πολλά ένζυμα καταλύουν τις χημικές αντιδράσεις χωρίς την βοήθεια των μετάλλων τους. Αντ’ αυτού, οι αντιδράσεις καταλύονται από ένα ή μερικά μεμονωμένα αμινοξέα στο ένζυμο. Ο έξυπνος προβληματισμός του Benjamin List ήταν: πρέπει τα αμινοξέα να αποτελούν μέρος ενός ενζύμου για να καταλύσουν μια χημική αντίδραση; ή θα μπορούσε ένα μόνο αμινοξύ, ή άλλα παρόμοια απλά μόρια, να κάνει την ίδια δουλειά;
Γνώριζε ότι υπήρχε έρευνα από τις αρχές της δεκαετίας του 1970 όπου το αμινοξύ προλίνη είχε χρησιμοποιηθεί ως καταλύτης – αλλά αυτό έγινε πριν από 25 και πλέον χρόνια. Αν η προλίνη ήταν όντως αποτελεσματικός καταλύτης, δεν θάπρεπε κάποιος να συνέχιζε τον πειραματισμό με αυτή;
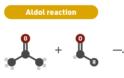
Ο Benjamin List υπέθεσε ότι ο λόγος για τον οποίο κανείς δεν συνέχισε να μελετά το φαινόμενο ήταν ότι δεν είχε λειτουργήσει ιδιαίτερα καλά. Με βαριά καρδιά, δοκίμασε αν η προλίνη θα μπορούσε να καταλύσει μια αντίδραση της αλδόλης, στην οποία άτομα άνθρακα από δύο διαφορετικά μόρια συνδέονται μεταξύ τους. Επρόκειτο για μια απλή προσπάθεια που για μεγάλη του έκπληξη λειτούργησε αμέσως.
Ο Benjamin List διεκδικεί το μέλλον του
Με τα πειράματά του, ο Benjamin List όχι μόνο απέδειξε ότι η προλίνη είναι ένας αποτελεσματικός καταλύτης, αλλά επίσης ότι αυτό το αμινοξύ μπορεί να οδηγήσει σε ασύμμετρη κατάλυση. Από τις δύο πιθανές εικόνες καθρέφτη, ήταν πολύ πιο συνηθισμένο να σχηματίζεται το ένα από το άλλο.
Σε αντίθεση με τους ερευνητές που είχαν προηγουμένως δοκιμάσει την προλίνη ως καταλύτη, ο Benjamin List συνειδητοποίησε τις τεράστιες δυνατότητες που θα μπορούσε να έχει. Σε σύγκριση με τα μέταλλα και τα ένζυμα, η προλίνη είναι ένα εκπληκτικό εργαλείο για τους χημικούς. Πρόκειται για ένα πολύ απλό, φθηνό και φιλικό προς το περιβάλλον μόριο. Όταν δημοσίευσε την ανακάλυψή του τον Φεβρουάριο του 2000, ο List περιέγραψε την ασύμμετρη κατάλυση με οργανικά μόρια ως μια νέα ιδέα με πολλές ευκαιρίες: «Ο σχεδιασμός και η διαλογή αυτών των καταλυτών είναι ένας από τους μελλοντικούς μας στόχους».
Ωστόσο, δεν ήταν μόνος σε αυτό. Σε ένα εργαστήριο βορειότερα στην Καλιφόρνια, ο David MacMillan δούλευε επίσης προς τον ίδιο στόχο.
Ο David MacMillan αφήνει πίσω τα μέταλλα Δύο χρόνια νωρίτερα, ο David MacMillan είχε μετακομίσει από το Harvard στο Berkeley. Στο Harvard είχε εργαστεί για τη βελτίωση της ασύμμετρης κατάλυσης χρησιμοποιώντας μέταλλα. Αυτός ήταν ένας τομέας που προσέλκυε την προσοχή πολλών ερευνητών, αλλά ο David MacMillan συνειδητοποίησε πώς οι καταλύτες που αναπτύσσονταν σπάνια χρησιμοποιούνταν στη βιομηχανία. Άρχισε να σκέφτεται το γιατί και υπέθεσε ότι τα ευαίσθητα μέταλλα ήταν απλώς δύσχρηστα και ακριβά στη χρήση. Η επίτευξη των συνθηκών χωρίς οξυγόνο και χωρίς υγρασία που απαιτούν ορισμένοι μεταλλικοί καταλύτες είναι σχετικά απλή σε ένα εργαστήριο, αλλά η διεξαγωγή βιομηχανικής παραγωγής μεγάλης κλίμακας σε τέτοιες συνθήκες είναι περίπλοκη.
Το συμπέρασμά του ήταν ότι για να είναι χρήσιμα τα χημικά εργαλεία που ανέπτυξε, χρειαζόταν μια αναθεώρηση. Έτσι, μετακομίζοντας στο Berkeley, άφησε πίσω του τα μέταλλα.
…για να αναπτύξει μια απλούστερη μορφή καταλύτη
Αντ’ αυτού, ο David MacMillan άρχισε να σχεδιάζει απλά οργανικά μόρια τα οποία – όπως και τα μέταλλα – θα μπορούσαν προσωρινά να παρέχουν ή να φιλοξενούν ηλεκτρόνια. Τα οργανικά μόρια είναι τα μόρια που χτίζουν όλα τα έμβια όντα. Η δομή των οργανικών μορίων καθορίζεται από άτομα άνθρακα τα οποία συνδέονται με χαρακτηριστικές ομάδες που περιέχουν συνήθως υδρογόνο, οξυγόνο, άζωτο, θείο ή φώσφορο.
Τα οργανικά μόρια αποτελούνται λοιπόν από απλά και κοινά στοιχεία, αλλά αναλόγως με το πώς διατάσσονται, μπορούν να έχουν πολύπλοκες ιδιότητες. Για να λειτουργήσει ως καταλύτης σε μια αντίδραση ένα οργανικό μόριο που ενδιέφερε τον David MacMillan, έπρεπε να είναι σε θέση να σχηματίσει ένα ιόν ιμινίου (iminium). Αυτό περιέχει ένα άτομο αζώτου, το οποίο έχει μια εγγενή συγγένεια για τα ηλεκτρόνια.
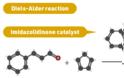
Επέλεξε αρκετά οργανικά μόρια με τις σωστές ιδιότητες και στη συνέχεια δοκίμασε την ικανότητά τους να οδηγούν μια αντίδραση Diels – Alder, την οποία οι χημικοί χρησιμοποιούν για να κατασκευάσουν δακτυλίους ατόμων άνθρακα. Όπως ακριβώς ήλπιζε και πίστευε, λειτούργησε εξαιρετικά. Ορισμένα από τα οργανικά μόρια ήταν επίσης εξαιρετικά στην ασύμμετρη κατάλυση. Από τα δυο πιθανά εναντιομερή, το ένα από αυτά προέκυπτε κατά 90% και πλέον στο τελικόν προϊόν.
Ο David MacMillan εφευρίσκει τον όρο οργανοκατάλυση
Όταν ο David MacMillan ήταν έτοιμος να δημοσιεύσει τα αποτελέσματά του, συνειδητοποίησε ότι η ιδέα για την κατάλυση που είχε ανακαλύψει χρειαζόταν ένα όνομα. Το γεγονός ήταν ότι οι ερευνητές είχαν προηγουμένως καταφέρει να καταλύσουν χημικές αντιδράσεις χρησιμοποιώντας μικρά οργανικά μόρια, αλλά αυτά ήταν μεμονωμένα παραδείγματα και κανείς δεν είχε συνειδητοποιήσει ότι η μέθοδος μπορούσε να γενικευτεί.
Ο David MacMillan ήθελε να βρει έναν όρο για να περιγράψει τη μέθοδο, ώστε άλλοι ερευνητές να καταλάβουν ότι υπήρχαν περισσότεροι οργανικοί καταλύτες για να ανακαλύψουν. Έτσι επέλεξε τον όρο οργανοκατάλυση.
Τον Ιανουάριο του 2000, λίγο πριν ο Benjamin List δημοσιεύσει την ανακάλυψή του, ο David MacMillan υπέβαλε το χειρόγραφο του για δημοσίευση σε επιστημονικό περιοδικό. Η εισαγωγή αναφέρει: «Εδώ, εισάγουμε μια νέα στρατηγική για την οργανοκατάλυση που αναμένουμε ότι θα είναι θετική σε μια σειρά ασύμμετρων μετασχηματισμών».
Η εξέλιξη της οργανοκατάλυσης
Ανεξάρτητα ο ένας από τον άλλο, οι Benjamin List και David MacMillan είχαν ανακαλύψει μια εντελώς νέα ιδέα για την κατάλυση. Από το 2000, οι εξελίξεις σε αυτόν τον τομέα ήταν καταιγιστικές. Σχεδιάστηκε πληθώρα φθηνών και σταθερών οργανοκαταλυτών, οι οποίοι μπορούν να χρησιμοποιηθούν ως καταλύτες σε μια τεράστια ποικιλία χημικών αντιδράσεων.
Οι οργανοκαταλύτες όχι μόνο αποτελούνται από απλά μόρια, σε ορισμένες περιπτώσεις μπορούν να λειτουργήσουν όπως ακριβώς και τα πολύπλοκα ένζυμα της φύσης. Με τους παλαιότερους καταλύτες στις διαδικασίες χημικής παραγωγής ήταν απαραίτητο να απομονωθεί και να καθαριστεί κάθε ενδιάμεσο προϊόν, διαφορετικά ο όγκος των υποπροϊόντων θα ήταν πολύ μεγάλος. Αυτό είχε ως αποτέλεσμα την απώλεια μέρους της ουσίας σε κάθε βήμα μιας χημικής κατασκευής. Οι οργανοκαταλύτες είναι πολύ πιο ανθεκτικοί καθώς, αρκετά βήματα σε μια διαδικασία παραγωγής μπορούν να εκτελεστούν χωρίς καμία διακοπή. Αυτό ονομάζεται αλυσιδωτή (ντόμινο) αντίδραση, η οποία μπορεί να μειώσει σημαντικά τα απόβλητα στην χημική παραγωγή.
Η σύνθεση της στρυχνίνης
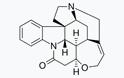
Το μόριο της στρυχνίνης
Ένα παράδειγμα του τρόπου με τον οποίο η οργανοκατάλυση οδήγησε σε πιο αποτελεσματικές μοριακές κατασκευές είναι η σύνθεση του φυσικού και εκπληκτικά πολύπλοκου μορίου στρυχνίνης. Πολλοί άνθρωποι συνάντησαν την στρυχνίνη ως δολοφονικό δηλητήριο στα αστυνομικά μυθιστορήματα της Αγκάθα Κρίστι. Ωστόσο, για τους χημικούς, η στρυχνίνη είναι κάτι σαν τον κύβο του Ρούμπικ: μια πρόκληση που θέλουμε να λύσουμε με όσο το δυνατόν λιγότερα βήματα.
Όταν η στρυχνίνη συντέθηκε για πρώτη φορά το 1952, απαιτούσε 29 διαφορετικές χημικές αντιδράσεις και μόνο το 0.0009% του αρχικού υλικού σχημάτισε στρυχνίνη. Τα υπόλοιπα χάθηκαν. Το 2011, οι ερευνητές μπόρεσαν να χρησιμοποιήσουν την οργανοκατάλυση και μια αντίδραση ντόμινο για να δημιουργήσουν στρυχνίνη σε μόλις 12 βήματα και η διαδικασία παραγωγής ήταν 7.000 φορές πιο αποδοτική.
Η οργανοκατάλυση στη φαρμακευτική παραγωγή
Η οργανοκατάλυση είχε σημαντικό αντίκτυπο στη φαρμακευτική έρευνα, η οποία συχνά απαιτεί ασύμμετρη κατάλυση. Μέχρι να μπορέσουν οι χημικοί να κάνουν ασύμμετρη κατάλυση, πολλά φαρμακευτικά προϊόντα περιείχαν και τα δυο εναντιομερή του μορίου. Όμως το ένα από αυτά ήταν αποτελεματικό, ενώ το άλλο θα μπορούσε μερικές φορές να έχει ανεπιθύμητα αποτελέσματα. Ένα τέτοιο τραγικό παράδειγμα ήταν η περίπτωση της θαλιδομίδης.
Την δεκαετία του 1950, η φαρμακευτική εταιρεία Γκρίνενταλ βρήκε ότι από ένα οργανικό μόριο μπορούσε να παραχθεί φάρμακο το οποίο καταπολεμούσε την πρωινή ναυτία των εγκύων. Το φάρμακο κυκλοφόρησε στο εμπόριο με το όνομα θαλιδομίδη. Αποδείχθηκε δημοφιλές προϊόν – μέχρι τη φρικιαστική ανακάλυψη ότι κάποιες μητέρες που το λάμβαναν γέννησαν παιδιά με παραμορφώσεις, όπως κοντά άκρα. Τελικά αποδείχθηκε ότι το τετραεδρικό μόριο που παρασκεύασε η Γκρίνενταλ, παρόλο που ήταν απολύτως ασφαλές και όντως κατέστειλε την πρωινή ναυτία, είχε κι ένα ιδιαίτερα επικίνδυνο εναντιομερές.
Χρησιμοποιώντας την οργανοκατάλυση, οι ερευνητές μπορούν πλέον με απλό τρόπο να παρασκευάσουν μεγάλες ποσότητες των κατάλληλων ασύμμετρων μορίων. Στις φαρμακευτικές εταιρείες, η μέθοδος χρησιμοποιείται επίσης για την βελτιστοποίηση της παραγωγής των υφιστάμενων φαρμακευτικών προϊόντων, όπως η παροξετίνη, η οποία χρησιμοποιείται για τη θεραπεία του άγχους και της κατάθλιψης, και το αντιικό φάρμακο Tamiflu, το οποίο χρησιμοποιείται για τη θεραπεία λοιμώξεων του αναπνευστικού.
Θα μπορούσαμε να απαριθμήσουμε χιλιάδες παραδείγματα για το πώς χρησιμοποιείται η οργανοκατάλυση. Πρόκειται για μια απλή, οικολογική και φθηνή μέθοδο κατάλυσης. Οι Benjamin List και David MacMillan ξεπέρασαν τις ισχυρές προκαταλήψεις που επικρατούσαν για το πώς καταλύονται οι χημικές αντιδράσεις. Πήγαν ένα βήμα πιο μακριά και αφήνοντας κατά μέρος τους γνωστούς καταλύτες, μέταλλα και ένζυμα, ανακάλυψαν τους οργανοκαταλύτες με τις αναρίθμητες εφαρμογές τους.
Ο BENJAMIN LIST γεννήθηκε το 1968 στην Φρανφούρτη στη Γερμανία. Έλαβε το διδακτορικό του το 1997 από το Goethe University Frankfurt. Είναι διευθυντής του Max-Planck-Institut für Kohlenforschung. Ο DAVID W.C. MACMILLAN γεννήθηκε το 1968 στους Bellshill της Σκωτίας. Έλαβε το διδακτορικό τους το 1996 από το Πανεπιστήμιο της California. Είναι καθηγητής στο Princeton.
πηγή: https://www.nobelprize.org/prizes/chemistry/2021/popular-information/
https://physicsgg.me/
tinanantsou.blogspot.gr
Η βιομηχανική παραγωγή και πολλά πεδία έρευνας εξαρτώνται από την ικανότητα των χημικών να κατασκευάζουν νέα και εξειδικευμένα μόρια. Αυτά μπορεί να είναι οτιδήποτε, από ουσίες που συλλαμβάνουν φως στα φωτοβολταϊκά ή αποθηκεύουν ενέργεια σε μπαταρίες, μέχρι μόρια που χρησιμεύουν στην κατασκευή ελαφρών αθλητικών παπουτσιών ή αποτελούν συστατικά φαρμάκων που θεραπεύουν. Ωστόσο, αν περιμέναμε από την φύση να δημιουργήσει τα εξειδικευμένα μόρια που μας είναι χρήσιμα θα είχαμε μείνει στην ‘λίθινη’ εποχή.
Είναι γεγονός ότι η φυσική εξέλιξη δημιούργησε εκπληκτικά εξειδικευμένα εργαλεία, τα ένζυμα. Τα ένζυμα στους ζωντανούς οργανισμούς χρησιμεύουν για την κατασκευή των μοριακών συμπλεγμάτων που δίνουν στη ζωή τα σχήματα, τα χρώματα και τις λειτουργίες της. Αρχικά, όταν οι χημικοί απομόνωσαν αυτά τα χημικά αριστουργήματα, απλώς τα κοίταξαν με θαυμασμό. Σήμερα όμως, μπορούμε να πούμε ότι οι χημικοί ξεπέρασαν την φύση όσον αφορά τα εξειδικευμένα εργαλεία για την κατασκευή μορίων.
Νέα εργαλεία για καλύτερη χημεία
Η ανακάλυψη που τιμήθηκε με το βραβείο Νόμπελ Χημείας 2021 οδήγησε την τεχνητή κατασκευή μορίων σε ένα εντελώς νέο επίπεδο. Δεν έκανε μόνο τη χημεία πιο οικολογική, αλλά βελτίωσε σημαντικά την παραγωγή ασύμμετρων μορίων.
Πολλά μόρια εμφανίζονται σε δύο παραλλαγές, με την μόνη διαφορά ότι είναι κατοπτρικά συμμετρικά – το ένα είναι το είδωλο του άλλου στον καθρέφτη. Υπάρχουν κι άλλα αντικείμενα που παρουσιάζουν αυτή τη σχέση ειδώλου προς αντικείμενο όπως π.χ. τα χέρια μας. Δεν μπορούμε να βάλουμε ακριβώς το δεξιό μας χέρι πάνω στο αριστερό – μόνο στον καθρέφτη ταιριάζουν απόλυτα. Τα σώματα αυτά ονομάζονται χειρόμορφα ή χειρικά. Στην χημεία χειρόμορφα μόρια ονομάζονται τα μόρια τα οποία δεν ταυτίζονται με το κατοπτρικό τους είδωλο. Αυτό σημαίνει ότι μια ένωση της οποίας το μόριο είναι χειρόμορφο εμφανίζεται σε δύο μορφές, τα εναντιομερή. Τα μόρια αυτά ενώ έχουν τον ίδιο μοριακό τύπο, εμφανίζουν διαφορές στις φυσικές και χημικές ιδιότητές τους. Αυτό είναι ένα είδος ισομέρειας – για την ακρίβεια στερεοϊσομέρειας – που ονομάζεται εναντιομέρεια. Για παράδειγμα τα εναντιομερή του λεμονένιου: η μια εκδοχή του μορίου λεμονένιου έχει άρωμα λεμονιού, ενώ το κατοπτρικό του είδωλο μυρίζει πορτοκάλι!
Κατά την χημική αντίδραση για την παραγωγή ενός μορίου προκύπτει συχνά μια κατάσταση όπου μπορούν να σχηματιστούν δύο μόρια με τον ίδιο μοριακό τύπο, τα οποία – όπως και τα χέρια μας – είναι κατοπτρικά συμμετρικά. Οι χημικοί συνήθως θέλουν μόνο το ένα από τα δύο, κυρίως όταν παράγουν φαρμακευτικά προϊόντα. Όμως, ήταν δύσκολο να βρεθούν αποτελεσματικές μέθοδοι για να γίνει αυτό. Η ιδέα που αναπτύχθηκε από τους Benjamin List και David MacMillan – η ασύμμετρη οργανοκατάλυση – είναι τόσο απλή όσο και ευφυής. Είναι γεγονός ότι πολλοί άνθρωποι αναρωτήθηκαν γιατί δεν το σκεφτήκαμε νωρίτερα. Αυτό δεν είναι εύκολο να απαντηθεί, αλλά πριν το επιχειρήσουμε θάπρεπε να κάνουμε μια γρήγορη αναδρομή στην ιστορία. Θα ορίσουμε τις έννοιες κατάλυση και καταλύτης που είναι βασικές για την κατανόηση του Νόμπελ Χημείας 2021.
Οι καταλύτες επιταχύνουν τις χημικές αντιδράσεις
Τον δέκατο ένατο αιώνα, όταν οι χημικοί άρχισαν να διερευνούν τους τρόπους με τους οποίους οι διαφορετικές χημικές ουσίες αντιδρούν μεταξύ τους, έκαναν μερικές παράξενες ανακαλύψεις. Για παράδειγμα, όταν έβαζαν άργυρο σε ένα ποτήρι με υπεροξείδιο του υδρογόνου (H2O2), το υπεροξείδιο του υδρογόνου άρχιζε ξαφνικά να διασπάται σε νερό (H2O) και οξυγόνο (O2). Αλλά ο άργυρος – που ξεκίνησε την χημική αντίδραση – δεν φαινόταν να επηρεαζόταν καθόλου από από αυτή. Η τελική του ποσότητα παράμενε εντελώς ίδια με την αρχική. Το 1835, ο διάσημος Σουηδός χημικός Jacob Berzelius διαπίστωσε κι άλλα τέτοια παραδειγματα.
Σύμφωνα με τα σχολικά βιβλία: Καταλύτης ονομάζεται μια ουσία, η οποία με την παρουσία του σε μικρά ποσά, αυξάνει την ταχύτητα μιας αντίδρασης, ενώ στο τέλος της αντίδρασης παραμένει ουσιαστικά αμετάβλητος τόσο στη μάζα όσο και στη χημική του σύσταση.
Έτσι, στην ετήσια έκθεση της Βασιλικής Σουηδικής Ακαδημίας Επιστημών, όπου περιέγραφε τις τελευταίες προόδους στη φυσική και την χημεία, αναφέρεται σε μια νέα «δύναμη» που μπορεί να «δημιουργήσει χημική δραστηριότητα». Παρέθεσε αρκετά παραδείγματα στα οποία απλώς η παρουσία μιας ουσίας ξεκινούσε μια χημική αντίδραση, αναφέροντας πώς αυτό το φαινόμενο πρέπει να είναι πολύ πιο συνηθισμένο από ό,τι πιστεύαμε. Θεωρούσε ότι η ουσία είχε καταλυτική δύναμη και ονόμασε το ίδιο το φαινόμενο κατάλυση.
Οι καταλύτες παράγουν πλαστικά, αρώματα και νόστιμα τρόφιμα
Από την εποχή του Berzelius μέχρι σήμερα κύλισε πολύ νερό μέσα από τους δοκιμαστικούς σωλήνες των χημικών. Ανακαλύφθηκε πληθώρα καταλυτών που μπορούν να διασπούν ή να ενώνουν μόρια μεταξύ τους, δημιουργώντας χιλιάδες διαφορετικές ουσίες που χρησιμοποιούνται στην καθημερινή μας ζωή, όπως φαρμακευτικά προϊόντα, πλαστικά, αρώματα και καρυκεύματα τροφίμων. Είναι γεγονός ότι το 35% του συνολικού παγκόσμιου ΑΕΠ περιλαμβάνει κατά κάποιο τρόπο την χημική κατάλυση.
Όλοι οι καταλύτες που είχαν ανακαλυφθεί πριν από το 2000 ανήκαν σε δύο ομάδες: ήταν είτε μέταλλα είτε ένζυμα. Τα μέταλλα είναι συχνά εξαιρετικοί καταλύτες επειδή έχουν την ικανότητα να δέχονται προσωρινά ηλεκτρόνια ή να τα παρέχουν σε άλλα μόρια κατά τη διάρκεια μιας χημικής διαδικασίας. Αυτό βοηθά στην χαλάρωση των δεσμών μεταξύ των ατόμων σε ένα μόριο, έτσι ώστε οι δεσμοί που κατά τα άλλα είναι ισχυροί να σπάσουν και να σχηματιστούν νέοι.
Ωστόσο, ένα πρόβλημα με ορισμένους μεταλλικούς καταλύτες είναι ότι είναι πολύ ευαίσθητοι στο οξυγόνο και στο νερό, οπότε, για να λειτουργήσουν, χρειάζονται ένα περιβάλλον χωρίς οξυγόνο και υγρασία. Αυτό είναι δύσκολο να επιτευχθεί σε βιομηχανίες μεγάλης κλίμακας. Επίσης, πολλοί μεταλλικοί καταλύτες είναι βαρέα μέταλλα, τα οποία μπορεί να είναι επιβλαβή για το περιβάλλον.
Οι καταλύτες της ζωής λειτουργούν με εκπληκτική ακρίβεια
Η δεύτερη μορφή καταλύτη είναι τα ένζυμα που αποτελούνται από πρωτεΐνες. Όλα τα έμβια όντα διαθέτουν χιλιάδες διαφορετικά ένζυμα που ενεργοποιούν και καθοδηγούν τις χημικές αντιδράσεις που είναι απαραίτητες για την ζωή. Η παρουσία των ενζύμων αυξάνει την ταχύτητα αυτών των αντιδράσεων έως και 100 εκατομμύρια φορές. Αυτό πρακτικά σημαίνει ότι αντιδράσεις που πραγματοποιούνται, με την παρουσία ενζύμων, μέσα σ’ ένα λεπτό, θα χρειάζονταν 32 μήνες για να πραγματοποιηθούν χωρίς αυτά.
Πολλά ένζυμα είναι εξειδικευμένα στην ασύμμετρη κατάλυση και επιτρέπουν πάντα εξ’ ορισμού τον σχηματισμό ενός από τα δυο εναντιομερή. Λειτουργούν επίσης και διαδοχικά – αν ένα ένζυμο τελειώσει με μια αντίδραση, ένα άλλο παίρνει την σκυτάλη. Με αυτόν τον τρόπο, δημιουργούν περίπλοκα μόρια με εκπληκτική ακρίβεια, όπως η χοληστερόλη, η χλωροφύλλη ή η τοξίνη που ονομάζεται στρυχνίνη, η οποία είναι ένα από τα πιο πολύπλοκα μόρια που γνωρίζουμε (θα επανέλθουμε σε αυτό).
Επειδή τα ένζυμα είναι τόσο αποτελεσματικοί καταλύτες, οι ερευνητές στη δεκαετία του 1990 προσπάθησαν να αναπτύξουν νέες παραλλαγές ενζύμων για να ελέγχουν τις χημικές αντιδράσεις που χρειάζεται η ανθρωπότητα. Η ερευνητική ομάδα που εργάστηκε σ’ αυτό καθοδηγήθηκε από τον Carlos F. Barbas III στο Ινστιτούτο Ερευνών Scripps στη νότια Καλιφόρνια. Ο Benjamin List κατείχε μια μεταδιδακτορική θέση στην ερευνητική ομάδα του Barbas όταν γεννήθηκε η λαμπρή ιδέα που οδήγησε σε μία από τις ανακαλύψεις που βρίσκεται πίσω από το φετινό Νόμπελ Χημείας.
Το επαναστατικό αποτέλεσμα της σκέψης του Benjamin List
Ο Benjamin List εργάστηκε με καταλυτικά αντισώματα. Κανονικά, τα αντισώματα προσκολλώνται σε ξένους ιούς ή βακτήρια στο σώμα μας, αλλά οι ερευνητές στο Scripps τα επανασχεδίασαν ώστε να μπορέσουν να προκαλέσουν χημικές αντιδράσεις.
Κατά την διάρκεια της εργασίας του με καταλυτικά αντισώματα, ο Benjamin List άρχισε να προβληματίζεται για το πώς πραγματικά λειτουργούν τα ένζυμα. Είναι συνήθως τεράστια μόρια που κατασκευάζονται από εκατοντάδες αμινοξέα. Εκτός από αυτά τα αμινοξέα, ένα σημαντικό ποσοστό ενζύμων έχει επίσης μέταλλα που βοηθούν στην επιτάχυνση των χημικών διεργασιών. Αλλά – κι εδώ είναι το ζουμί – πολλά ένζυμα καταλύουν τις χημικές αντιδράσεις χωρίς την βοήθεια των μετάλλων τους. Αντ’ αυτού, οι αντιδράσεις καταλύονται από ένα ή μερικά μεμονωμένα αμινοξέα στο ένζυμο. Ο έξυπνος προβληματισμός του Benjamin List ήταν: πρέπει τα αμινοξέα να αποτελούν μέρος ενός ενζύμου για να καταλύσουν μια χημική αντίδραση; ή θα μπορούσε ένα μόνο αμινοξύ, ή άλλα παρόμοια απλά μόρια, να κάνει την ίδια δουλειά;
Γνώριζε ότι υπήρχε έρευνα από τις αρχές της δεκαετίας του 1970 όπου το αμινοξύ προλίνη είχε χρησιμοποιηθεί ως καταλύτης – αλλά αυτό έγινε πριν από 25 και πλέον χρόνια. Αν η προλίνη ήταν όντως αποτελεσματικός καταλύτης, δεν θάπρεπε κάποιος να συνέχιζε τον πειραματισμό με αυτή;
Ο Benjamin List υπέθεσε ότι ο λόγος για τον οποίο κανείς δεν συνέχισε να μελετά το φαινόμενο ήταν ότι δεν είχε λειτουργήσει ιδιαίτερα καλά. Με βαριά καρδιά, δοκίμασε αν η προλίνη θα μπορούσε να καταλύσει μια αντίδραση της αλδόλης, στην οποία άτομα άνθρακα από δύο διαφορετικά μόρια συνδέονται μεταξύ τους. Επρόκειτο για μια απλή προσπάθεια που για μεγάλη του έκπληξη λειτούργησε αμέσως.
Ο Benjamin List διεκδικεί το μέλλον του
Με τα πειράματά του, ο Benjamin List όχι μόνο απέδειξε ότι η προλίνη είναι ένας αποτελεσματικός καταλύτης, αλλά επίσης ότι αυτό το αμινοξύ μπορεί να οδηγήσει σε ασύμμετρη κατάλυση. Από τις δύο πιθανές εικόνες καθρέφτη, ήταν πολύ πιο συνηθισμένο να σχηματίζεται το ένα από το άλλο.
Σε αντίθεση με τους ερευνητές που είχαν προηγουμένως δοκιμάσει την προλίνη ως καταλύτη, ο Benjamin List συνειδητοποίησε τις τεράστιες δυνατότητες που θα μπορούσε να έχει. Σε σύγκριση με τα μέταλλα και τα ένζυμα, η προλίνη είναι ένα εκπληκτικό εργαλείο για τους χημικούς. Πρόκειται για ένα πολύ απλό, φθηνό και φιλικό προς το περιβάλλον μόριο. Όταν δημοσίευσε την ανακάλυψή του τον Φεβρουάριο του 2000, ο List περιέγραψε την ασύμμετρη κατάλυση με οργανικά μόρια ως μια νέα ιδέα με πολλές ευκαιρίες: «Ο σχεδιασμός και η διαλογή αυτών των καταλυτών είναι ένας από τους μελλοντικούς μας στόχους».
Ωστόσο, δεν ήταν μόνος σε αυτό. Σε ένα εργαστήριο βορειότερα στην Καλιφόρνια, ο David MacMillan δούλευε επίσης προς τον ίδιο στόχο.
Ο David MacMillan αφήνει πίσω τα μέταλλα Δύο χρόνια νωρίτερα, ο David MacMillan είχε μετακομίσει από το Harvard στο Berkeley. Στο Harvard είχε εργαστεί για τη βελτίωση της ασύμμετρης κατάλυσης χρησιμοποιώντας μέταλλα. Αυτός ήταν ένας τομέας που προσέλκυε την προσοχή πολλών ερευνητών, αλλά ο David MacMillan συνειδητοποίησε πώς οι καταλύτες που αναπτύσσονταν σπάνια χρησιμοποιούνταν στη βιομηχανία. Άρχισε να σκέφτεται το γιατί και υπέθεσε ότι τα ευαίσθητα μέταλλα ήταν απλώς δύσχρηστα και ακριβά στη χρήση. Η επίτευξη των συνθηκών χωρίς οξυγόνο και χωρίς υγρασία που απαιτούν ορισμένοι μεταλλικοί καταλύτες είναι σχετικά απλή σε ένα εργαστήριο, αλλά η διεξαγωγή βιομηχανικής παραγωγής μεγάλης κλίμακας σε τέτοιες συνθήκες είναι περίπλοκη.
Το συμπέρασμά του ήταν ότι για να είναι χρήσιμα τα χημικά εργαλεία που ανέπτυξε, χρειαζόταν μια αναθεώρηση. Έτσι, μετακομίζοντας στο Berkeley, άφησε πίσω του τα μέταλλα.
…για να αναπτύξει μια απλούστερη μορφή καταλύτη
Αντ’ αυτού, ο David MacMillan άρχισε να σχεδιάζει απλά οργανικά μόρια τα οποία – όπως και τα μέταλλα – θα μπορούσαν προσωρινά να παρέχουν ή να φιλοξενούν ηλεκτρόνια. Τα οργανικά μόρια είναι τα μόρια που χτίζουν όλα τα έμβια όντα. Η δομή των οργανικών μορίων καθορίζεται από άτομα άνθρακα τα οποία συνδέονται με χαρακτηριστικές ομάδες που περιέχουν συνήθως υδρογόνο, οξυγόνο, άζωτο, θείο ή φώσφορο.
Τα οργανικά μόρια αποτελούνται λοιπόν από απλά και κοινά στοιχεία, αλλά αναλόγως με το πώς διατάσσονται, μπορούν να έχουν πολύπλοκες ιδιότητες. Για να λειτουργήσει ως καταλύτης σε μια αντίδραση ένα οργανικό μόριο που ενδιέφερε τον David MacMillan, έπρεπε να είναι σε θέση να σχηματίσει ένα ιόν ιμινίου (iminium). Αυτό περιέχει ένα άτομο αζώτου, το οποίο έχει μια εγγενή συγγένεια για τα ηλεκτρόνια.
Επέλεξε αρκετά οργανικά μόρια με τις σωστές ιδιότητες και στη συνέχεια δοκίμασε την ικανότητά τους να οδηγούν μια αντίδραση Diels – Alder, την οποία οι χημικοί χρησιμοποιούν για να κατασκευάσουν δακτυλίους ατόμων άνθρακα. Όπως ακριβώς ήλπιζε και πίστευε, λειτούργησε εξαιρετικά. Ορισμένα από τα οργανικά μόρια ήταν επίσης εξαιρετικά στην ασύμμετρη κατάλυση. Από τα δυο πιθανά εναντιομερή, το ένα από αυτά προέκυπτε κατά 90% και πλέον στο τελικόν προϊόν.
Ο David MacMillan εφευρίσκει τον όρο οργανοκατάλυση
Όταν ο David MacMillan ήταν έτοιμος να δημοσιεύσει τα αποτελέσματά του, συνειδητοποίησε ότι η ιδέα για την κατάλυση που είχε ανακαλύψει χρειαζόταν ένα όνομα. Το γεγονός ήταν ότι οι ερευνητές είχαν προηγουμένως καταφέρει να καταλύσουν χημικές αντιδράσεις χρησιμοποιώντας μικρά οργανικά μόρια, αλλά αυτά ήταν μεμονωμένα παραδείγματα και κανείς δεν είχε συνειδητοποιήσει ότι η μέθοδος μπορούσε να γενικευτεί.
Ο David MacMillan ήθελε να βρει έναν όρο για να περιγράψει τη μέθοδο, ώστε άλλοι ερευνητές να καταλάβουν ότι υπήρχαν περισσότεροι οργανικοί καταλύτες για να ανακαλύψουν. Έτσι επέλεξε τον όρο οργανοκατάλυση.
Τον Ιανουάριο του 2000, λίγο πριν ο Benjamin List δημοσιεύσει την ανακάλυψή του, ο David MacMillan υπέβαλε το χειρόγραφο του για δημοσίευση σε επιστημονικό περιοδικό. Η εισαγωγή αναφέρει: «Εδώ, εισάγουμε μια νέα στρατηγική για την οργανοκατάλυση που αναμένουμε ότι θα είναι θετική σε μια σειρά ασύμμετρων μετασχηματισμών».
Η εξέλιξη της οργανοκατάλυσης
Ανεξάρτητα ο ένας από τον άλλο, οι Benjamin List και David MacMillan είχαν ανακαλύψει μια εντελώς νέα ιδέα για την κατάλυση. Από το 2000, οι εξελίξεις σε αυτόν τον τομέα ήταν καταιγιστικές. Σχεδιάστηκε πληθώρα φθηνών και σταθερών οργανοκαταλυτών, οι οποίοι μπορούν να χρησιμοποιηθούν ως καταλύτες σε μια τεράστια ποικιλία χημικών αντιδράσεων.
Οι οργανοκαταλύτες όχι μόνο αποτελούνται από απλά μόρια, σε ορισμένες περιπτώσεις μπορούν να λειτουργήσουν όπως ακριβώς και τα πολύπλοκα ένζυμα της φύσης. Με τους παλαιότερους καταλύτες στις διαδικασίες χημικής παραγωγής ήταν απαραίτητο να απομονωθεί και να καθαριστεί κάθε ενδιάμεσο προϊόν, διαφορετικά ο όγκος των υποπροϊόντων θα ήταν πολύ μεγάλος. Αυτό είχε ως αποτέλεσμα την απώλεια μέρους της ουσίας σε κάθε βήμα μιας χημικής κατασκευής. Οι οργανοκαταλύτες είναι πολύ πιο ανθεκτικοί καθώς, αρκετά βήματα σε μια διαδικασία παραγωγής μπορούν να εκτελεστούν χωρίς καμία διακοπή. Αυτό ονομάζεται αλυσιδωτή (ντόμινο) αντίδραση, η οποία μπορεί να μειώσει σημαντικά τα απόβλητα στην χημική παραγωγή.
Η σύνθεση της στρυχνίνης
Το μόριο της στρυχνίνης
Ένα παράδειγμα του τρόπου με τον οποίο η οργανοκατάλυση οδήγησε σε πιο αποτελεσματικές μοριακές κατασκευές είναι η σύνθεση του φυσικού και εκπληκτικά πολύπλοκου μορίου στρυχνίνης. Πολλοί άνθρωποι συνάντησαν την στρυχνίνη ως δολοφονικό δηλητήριο στα αστυνομικά μυθιστορήματα της Αγκάθα Κρίστι. Ωστόσο, για τους χημικούς, η στρυχνίνη είναι κάτι σαν τον κύβο του Ρούμπικ: μια πρόκληση που θέλουμε να λύσουμε με όσο το δυνατόν λιγότερα βήματα.
Όταν η στρυχνίνη συντέθηκε για πρώτη φορά το 1952, απαιτούσε 29 διαφορετικές χημικές αντιδράσεις και μόνο το 0.0009% του αρχικού υλικού σχημάτισε στρυχνίνη. Τα υπόλοιπα χάθηκαν. Το 2011, οι ερευνητές μπόρεσαν να χρησιμοποιήσουν την οργανοκατάλυση και μια αντίδραση ντόμινο για να δημιουργήσουν στρυχνίνη σε μόλις 12 βήματα και η διαδικασία παραγωγής ήταν 7.000 φορές πιο αποδοτική.
Η οργανοκατάλυση στη φαρμακευτική παραγωγή
Η οργανοκατάλυση είχε σημαντικό αντίκτυπο στη φαρμακευτική έρευνα, η οποία συχνά απαιτεί ασύμμετρη κατάλυση. Μέχρι να μπορέσουν οι χημικοί να κάνουν ασύμμετρη κατάλυση, πολλά φαρμακευτικά προϊόντα περιείχαν και τα δυο εναντιομερή του μορίου. Όμως το ένα από αυτά ήταν αποτελεματικό, ενώ το άλλο θα μπορούσε μερικές φορές να έχει ανεπιθύμητα αποτελέσματα. Ένα τέτοιο τραγικό παράδειγμα ήταν η περίπτωση της θαλιδομίδης.
Την δεκαετία του 1950, η φαρμακευτική εταιρεία Γκρίνενταλ βρήκε ότι από ένα οργανικό μόριο μπορούσε να παραχθεί φάρμακο το οποίο καταπολεμούσε την πρωινή ναυτία των εγκύων. Το φάρμακο κυκλοφόρησε στο εμπόριο με το όνομα θαλιδομίδη. Αποδείχθηκε δημοφιλές προϊόν – μέχρι τη φρικιαστική ανακάλυψη ότι κάποιες μητέρες που το λάμβαναν γέννησαν παιδιά με παραμορφώσεις, όπως κοντά άκρα. Τελικά αποδείχθηκε ότι το τετραεδρικό μόριο που παρασκεύασε η Γκρίνενταλ, παρόλο που ήταν απολύτως ασφαλές και όντως κατέστειλε την πρωινή ναυτία, είχε κι ένα ιδιαίτερα επικίνδυνο εναντιομερές.
Χρησιμοποιώντας την οργανοκατάλυση, οι ερευνητές μπορούν πλέον με απλό τρόπο να παρασκευάσουν μεγάλες ποσότητες των κατάλληλων ασύμμετρων μορίων. Στις φαρμακευτικές εταιρείες, η μέθοδος χρησιμοποιείται επίσης για την βελτιστοποίηση της παραγωγής των υφιστάμενων φαρμακευτικών προϊόντων, όπως η παροξετίνη, η οποία χρησιμοποιείται για τη θεραπεία του άγχους και της κατάθλιψης, και το αντιικό φάρμακο Tamiflu, το οποίο χρησιμοποιείται για τη θεραπεία λοιμώξεων του αναπνευστικού.
Θα μπορούσαμε να απαριθμήσουμε χιλιάδες παραδείγματα για το πώς χρησιμοποιείται η οργανοκατάλυση. Πρόκειται για μια απλή, οικολογική και φθηνή μέθοδο κατάλυσης. Οι Benjamin List και David MacMillan ξεπέρασαν τις ισχυρές προκαταλήψεις που επικρατούσαν για το πώς καταλύονται οι χημικές αντιδράσεις. Πήγαν ένα βήμα πιο μακριά και αφήνοντας κατά μέρος τους γνωστούς καταλύτες, μέταλλα και ένζυμα, ανακάλυψαν τους οργανοκαταλύτες με τις αναρίθμητες εφαρμογές τους.
Ο BENJAMIN LIST γεννήθηκε το 1968 στην Φρανφούρτη στη Γερμανία. Έλαβε το διδακτορικό του το 1997 από το Goethe University Frankfurt. Είναι διευθυντής του Max-Planck-Institut für Kohlenforschung. Ο DAVID W.C. MACMILLAN γεννήθηκε το 1968 στους Bellshill της Σκωτίας. Έλαβε το διδακτορικό τους το 1996 από το Πανεπιστήμιο της California. Είναι καθηγητής στο Princeton.
πηγή: https://www.nobelprize.org/prizes/chemistry/2021/popular-information/
https://physicsgg.me/
tinanantsou.blogspot.gr
ΦΩΤΟΓΡΑΦΙΕΣ
ΜΟΙΡΑΣΤΕΙΤΕ
ΔΕΙΤΕ ΑΚΟΜΑ
ΠΡΟΗΓΟΥΜΕΝΟ ΑΡΘΡΟ
Δείτε τα νούμερα τηλεθέασης (18/54) στη μεσημεριανή ζώνη! (8/10/2021)
ΣΧΟΛΙΑΣΤΕ